Наследственная энзимопеническая метгемоглобинемия – наследственное заболевание, при котором содержание метгемоглобина (MetHb) в крови превышает физиологическую норму (> 1–2% общего количества Hb) (Казанец Е.Г., 2009). В России наблюдается преимущественно у взрослых в виде эндемических очагов в Якутии в районе реки Вилюй (Токарев Ю.Н. и соавт., 1975, 1976, 1983; Дервиз Г.В., 1977; Нисан Л.Г. и соавт.,1987). Выраженность симптомов обусловлена количеством метгемоглобина в крови. Повышение MetHb до 10% чаще всего не дает клинически выраженных проявлений. При повышении MetHb в пределах 10–20% появляется цианоз слизистых и кожных покровов, возникают общая слабость, недомогание, ослабление памяти, раздражительность, головные боли. При содержании MetHb в пределах 30–50% к вышеперечисленным симптомам присоединяются боли в сердце различного характера, одышка, головокружение, резко выраженный цианоз, повышенная вязкость крови. Содержание MetHb более 70% несовместимо с жизнью.
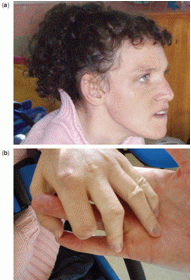 | Симптомы:
a) умеренный цианоз губ и слизистой рта, проявления дистонии в мышцах лица;
b) цианоз ногтевых пластинок.
При метгемоглобинемии 1 типа пациентов периодически беспокоят головные боли, головокружение, одышка, тахикардия, быстрая утомляемость, сонливость, возможно, отставание в физическом и психическом развитии.
При метгемоглобинемии 2 типа цианоз сопровождается задержкой интеллектуального развития, прогрессирующей вторичной микроцефалией, нарушением развития нервной системы.МРТ часто обнаруживает корковую и подкорковую атрофию.
Лабораторные методы исследования выявляют повышение содержания метгемоглобина (1540%) и количества эритроцитов (компенсаторный эритроцитоз).
|
Молекулярно-генетическая причина заболевания - мутации в гене DIAI, кодирующем две формы фермента NADH-цитохром b5 редуктазы. Мембраносвязанная форма фермента участвует в основных биохимических процессах каждой клетки, растворимая форма участвует в редукции метгемоглобина в эритрорцитах. При мутациях, приводящих к нарушению работы только растворимой формы фермента, возникает 1-ый тип заболевания. При мутациях, нарушающих функционирование обоих форм фермента - второй тип. В России метгемоглобинемия первого типа наиболее часто встречается среди народа саха, частота его в Якутии составляет 1:5700 человек, т.е. каждый 37 якут является гетерозиготным носителем заболевания.Молекулярно-генетической причиной заболевания якутского варианта метгемоглобинемии 1 типа является мутация с.806С›Т в гене DIA1, приводящая к аминокислотной замене Pro269Leu.
Роль красных клеток крови в метаболизме метгемоглобина была установлена Gibson QH в 1943-48 годах. Согласно современным взглядам в эритроцитах одновременно происходит две противоположные реакции, уравновешивающие друг друга. С одной стороны, железо гемоглобина окисляется, превращаясь из двухвалентного в трёхвалентное, при этом образуется не переносящий кислород метгемоглобин (MetHb), за сутки его образуется 0,5-3% от общего количества гемоглобина в организме (Дервиз Г.В., 1977). С другой стороны этот MetHb всё время восстанавливается обратно в функционально активный гемоглобин, в итоге у здоровых людей уровень MetHb удерживается в пределах до 1-1,5%. Процесс восстановления MetHb в эритроцитах изучен довольно хорошо. В эритроцитах известно несколько далеко не равноценных по своей эффективности восстанавливающих систем. 67-73% восстановления MetHb в активный Hb обеспечивает фермент эритроцитов NADH-cytochromeb5 reductase (НАД·Н2-MetHb-редуктаза, NADH-феррицианидредуктаза, NADH-дегидрогеназа, диафораза I, NADH-дегидрогеназа, его роль установлена в 1959 Scott and Griffith). При блокаде этой системы вследствие генетических дефектов стимулируются минорные пути прямого восстановления MetHb эндогенными восстановителями (аскорбиновой кислотой, восстановленным глютатионом, флавином, тетрагидроптерином, цистеином, метаболитами триптофана) или другими системами (Казанец Е.Г., 2009).
Наследственная энзимопеническая метгемоглобинемия (НЭМ), или метгемоглобинемия, обусловленная дефицитом НАДН-цитохром-Ьб-редуетазы (ММ 250800) до сих пор остается мало изученной патологией, особенно у детей (Jaffe E R., 1986; Shirabe К., Yubisui T., 1991; Wu Y., Mota L.V., Kaplan J.C., 1995; Chang-Hui Huang, 1998; Dekker J., Eppink M., 2001). Патогенез клинических проявлений НЭМ определяется хронической гипоксией вследствие окисления части гемоглобина в мет-форму и образования «валентных» гибридов, не способных захватывать кислород в легких и доставлять его тканям (Андреева А.П., 1976, 1977; Захарова Ф.А., 1982; Токарев Ю.Н., 1983). Степень выраженности клинической симптоматики зависит от содержания метгемоглобина в крови и компенсаторных способностей сердечно-сосудистой, дыхательной и гемопоэтической систем в процессе адаптации к гипоксии (Кушаковский М.С., 1968; Ниссан Л.Г., 1987; Аскерова Т.А., 1995).
В литературе имеются описания клинической картины заболевания и состояния периферической крови у взрослых (Захарова Ф.А., 1982; Токарев Ю.Н., 1983; Jenkins J.M., 1992; Shirabe К., 1995; Wang Y., Wu Y., 2000). При этом установлено увеличение содержания гемоглобина, эритроцитов, очевидно, носящее компенсаторный характер (Токарев Ю. Н., 1980, 1983). Захарова Ф.А. (1982) сообщает о повышении уровня сывороточного железа у больных. Однако в литературе нет данных о функционально-морфологическом состоянии периферического звена эритрона при этом заболевании. Имеются лишь единичные сведения об изменениях морфологической характеристики эритроцитов при различных гемоглобинопатиях, сопровождающихся гипоксией (Ковалева Л.Г., Постников Ю.В., 1987; Казанец Е.Г.,1990; Троицкая О.В.,1996, 1999; Nagai Т., 1980).
Клиническая картина наследственной энзиматической метгемоглобинемии у детей имеет возрастные особенности: для школьников характерен более выраженный цианоз, симптомы функциональной кардиопатии и гипоксии. Показатели массы тела и роста у детей с наследственной энзимопенической метгемоглобинемей ниже средних показателей, причем их дефицит увеличивается с возрастом. Периферическое звено эритрона у больных независимо от возраста характеризуется увеличением числа незрелых форм эритроцитов, а также значительным увеличением дегенеративных и плоских форм эритроцитов. Пациенты с наследственной энзимопенической метгемоглобинемей независимо от возраста имели усиление перекисного окисления липидов и снижение активности антиоксидантных систем - каталазы и низкомолекулярных антиоксидантов. Для младшей группы детей характерно увеличение супероксиддисмутазы. Патогенетическая терапия аскорбиновой кислотой приводит к улучшению . состояния детей, снижению уровня метгемоглобина и повышению активности суммарных антиоксидантов.
Течение болезни, как правило, доброкачественное. Продолжительность жизни пациентов не страдает. Кровь у таких больных темно-коричневого цвета в результате повышения содержания метгемоглобина. В некоторых случаях у нелеченых больных может наблюдаться вторичный компенсаторный эритроцитоз, увеличение содержания гемоглобина (до 170240 г/л), небольшой ретикулоцитоз (менее 3%), повышение вязкости крови и уменьшение СОЭ. Возможно незначительное повышение билирубина в сыворотке крови за счет непрямой (свободной) фракции. У гетерозигот концентрация метгемоглобина в крови составляет 12%, признаки заболевания отсутствуют. Цианоз может появиться после приема метгемоглобинобразующих лекарственных препаратов (Трошин В.А., 2007; Казанец Е.Г., 2009).
В Якутии зарегистрировано необычайно высокое распространение НЭМ I типа у коренных жителей республики (Токарев Ю.Н., 1983, где) частота её составляет 1:5700 человек, т.е. каждый 37 якут является гетерозиготным носителем заболевания. По сути дела, Якутия является единственным очагом данного заболевания на территории России. (За пределами России наследственные доброкачественные метгемоглобинемии распространены среди жителей Гренландии, индейцев Аляски и представителей племени навахос в США).
Возможно, что накопление этого заболевания произошло вследствие эффекта основателя - популяционно-генетического феномена, связанного с ограниченной репродуктивной численностью в прошлом достаточно изолированных популяций (Серошевский В.Л. 1993). Молекулярно-генетическое исследование якутских больных с НЭМ не подтвердило наличие 3 точковых мутаций гена НАДН-цитохром-Ь5-редуктазы (А^5701п, Ьеи72Рго, Уа1105Ме1), встречающихся на территории Азии у японцев и китайцев.
Литература
- Блюменфельд Л.А. Гемоглобин и обратимое присоединение кислорода. М.: Сов. наука, 1957.
- Дервиз Г.В. Наследственная энзимопеническая метгемоглобинемия.//Клиническая медицина, 1977, №5, стр. 8.
- Казанец Е.Г. Метгемоглобинемии.// Детская больница, 2009, №1, стр. 38-42.
- Казанец Е.Г., Андреева А.П., Хангулов С.В., Токарев Ю.Н. Наследственные цианозы, обусловленные присутствием в крови аномальных гемоглобинов группы М: выявление, идентификация, свойства // Гематология и трансфузиология, 1990, №3, с. 9–13.
- Краснопольская К.Д. Наследственные болезни обмена веществ. – М., 2005, 290 с.
- Мельник А.И., Мельник В.А. Обострение наследственной метгемоглобинемии у близнецов грудного возраста//Педиатрия. - 1986. - № 12. - С. 58 - 60.
- Нисан Л.Г., Гуревич С.П., Казанец Е.Г., Фролова М.И., Токарев Ю.Н., Салмова Т.С., Бутина М.В. Наследственная энзимопеническая метгемоглобинемия у новорожденных // Вопросы материнства и детства, 1987, №1, с. 74–75.
- Токарев Ю.Н., Файнштейн Ф.Э. и др.//Проблемы гематологии и трансфузиологии. Т.2. М., 1976, С.123-128.
- Токарев Ю.Н., Холлан С.Р., Корраля-Альмонте Х.С.// Наследственные анемии и гемоглобинопатии. – М., 1983.
- Торшин В. А. Клинически значимые дисгмоглобины. Карбоксигемоглобин // Лаборатория. 2007. № 1. С. 17-18.
- Челноков С.Б., Яковлева Е.А., Пудина Н.А. Случай тяжелой метгемоглобинемии у недоношенного новорожденного ребенка// Вестник интенсивной терапии. 2002. №2. С.1821.
- Aalfs CM, Salieb-Beugelaar GB, Wanders RJ, Mannens MM, Wijburg FA. A case of methemoglobinemia type II due to NADH-cytochrome b5 reductase deficiency: determination of the molecular basis. Hum Mutat 2000;16:18–22.
- Abdemoula MS. La methemoglobinemia hereditaire recessive de type II. A propos d’une observation. Revue Maghrebine de Pediatrie 2002; XII-IV:207–10.
- Bewley MC, Davis CA, Marohnic CC, Taormina D, Barber MJ. The structure of the S127P mutant of cytochrome b5 reductase that causes methemoglobinemia shows the AMP moiety of the flavin occupying the substrate binding site. Biochemistry 2003; 42:13145–51.
- Blumenfeld L.A. Physics of Bioenergetic Processes. N.Y.: Springer-Verlag, 1983.
- Davis CA, Barber MJ. Cytochrome b5 oxidoreductase: expression and characterization of the original familial idiopathic methemoglobinemia mutations E255 and G291D. Arch Biochem Biophys 2004; 425:123–32.
- Dekker J, Eppink MH , van Zwieten R, de Rijk T, Remacha AF, Law LK, et al. Seven new mutations in the nicotinamide adenine dinucleotide reduced-cytochrome b(5) reductase gene leading to methemoglobinemia type I. Blood 2001;97:1106–14.
- Den Dunnen JT, Antonarakis SE. Mutation nomenclature extensions and suggestions to describe complex mutations: a discussion. Hum Mutat 2000;15:7–12.
- Dickerson R. E., Geis I. Hemoglobin: Structure, Function, Evolution, and Pathology (Benjamin Cummings: Menlo Park, CA), 1983.
- Du M, Shirabe K, Takeshita M. Identification of alternative first exons of NADH-cytochrome b5 reductase gene expressed ubiquitously in human cells. Biochem Biophys Res Commun1997; 235:779–83.
- Ewenczyk C., Leroux A., Roubergue A., Laugel V., Afenjar A., Saudubray J.M., Beauvais P., BillettedeVillemeur T., Vidailhet M., Roze E. Recessive hereditary methaemoglobinaemia, typeII: delineation of the clinical spectrum./ Brain (2008), 131,760-771.
- Fermo E, Bianchi P, Vercellati C, et al. Recessive hereditary methemoglobinemia: Two novel mutations in the NADH-cytochrome b5 reductase gene. /J Blood Cells Mol Dis 2008 Mar 15.
- Fisher RA, Povey S, Bobrow M, Solomon E, Boyd Y, Carritt B. Assignment of the DIA1locus to chromosome 22.Ann Hum Genet 1977;41:151–5.
- Francois. Cas de cyanose conge?nitale sans cause apparente. Bull Acad. Roy Med Belg 1845; 4: 698.
- Fusco C, Soncini G, Frattini D, Giustina ED, Vercellati C, Fermo E, Bianchi P. Cerebellar atrophy in a child with hereditary methemoglobinemia type II./ Brain Dev 2010 Jul 21.
- Gibson QH. The reduction of methaemoglobin in red blood cells and studies on the cause of idiopathic methaemoglobinaemia. Biochem J 1948; 42:13–23.
- Gokalp S, Unuvar E, Oguz F, Kilic A, Sidal M. A case with quadriparetic cerebral palsy and cyanosis: congenital methemoglobinemia. Pediatr Neurol 2005; 33:131–3.
- Gonzalez R, Estrada M, Wade M, de la Torre E, Svarch E, Fernandez O, et al. Heterogeneity of hereditary methaemoglobinaemia: a study of 4 Cuban families with NADH-Methaemoglobin reductase deficiency including a new variant (Santiago de Cuba variant). Scand J Haematol 1978; 20:385–93.
- Grabowska D, Plochocka D, Jablonska-Skwiecinska E, Chelstowska A, Lewandowska I, Staniszewska K, et al. Compound heterozygosity of two missense mutations in the NADH-cytochrome b5 reductase gene of a Polish patient with type I recessive congenital methaemoglobinaemia. Eur J Haematol 2003; 70:404–9.
- Guex N, Peitsch MC. SWISS-MODEL and the Swiss-PdbViewer: an environment for comparative protein modeling. Electrophoresis 1997; 18: 2714–23.
- Hegesh E, Hegesh J, Kaftory A. Congenital methemoglobinemia with a deficiency of cytochrome b5. N Engl J Med. 1986; 314:757–761.
- Heusden A, Willems C, Lambotte C,Hainaut H, Chapelle P, Malchair R. [Hereditary methemoglobinemia with mental retardation. Study of 3 further cases]. Arch Fr Pediatr 1971; 28: 631–45.
- Higasa K, Manabe JI, Yubisui T,Sumimoto H, Pung-Amritt P, Tanphaichitr VS, et al. Molecular basis of hereditary methaemoglobinaemia, types I and II: two novel mutations in the NADH-cytochrome b5 reductase gene. Br J Haematol 1998; 103: 922–30.
- Hildebrandt A, Estabrook RW. Evidence for the participation of cytochrome b 5 in hepatic microsomal mixed-function oxidation reactions. Arch Biochem Biophys 1971; 143: 66–79.
- Hirono H. Lipids of liver, kidney, spleen and muscle in a case of generalized deficiency of cytochrome b5 reductase in congenital methemoglobinemia with mental retardation. Lipids 1984; 19: 60–3.
- Hitzenberger K. Autotoxische zyanose (intraglobulare methamoglobinamie). Wien Arch Intern Med.1932;23:85.
- Hultquist DE, Passon PG. Catalysis of methaemoglobin reduction by erythrocyte cytochrome b5 and cytochrome b5 reductase. Nature1971; 229: 252–4.
- Jablonska-Skwiecinska E, Holtorp-Tyszkiewiczowa J, Staniszewska K. Generalized deficiency of the NADH-methemoglobin reductase in congenital methemoglobinemia with neurological symptoms. Biomed Biochim Acta 1984; 43: S98–100.
- Jaffe ER, Hultquist DE. Cytochrome b5 reductase deficiency and Enzymopenic hereditary methemoglobinemia. In: Scriver CR, Beaudet AL, Sly WS, et al, eds. The Metabolic and Molecular Basis of Inherited Disease.7th ed. NewYork, NY: McGraw-Hill;1995:2267–2280.
- Junien C, Leroux A, Lostanlen D, Reghis A, Boue J, Nicolas H, et al. Prenatal diagnosis of congenital Enzymopenic methaemoglobinaemia with mental retardation due to generalized cytochrome b5 reductase deficiency: firstre port of two cases. Prenat Diagn 1981; 1: 17–24.
- Kaftory A, Freundlich E, Manaster J, Shukri A, Hegesh E. Prenatal Diagnosis of congenital methemoglobinemia with mental retardation. Isr J Med Sci 1986; 22: 837–40.
- Kobayashi Y, Fukumaki Y, Yubisui T, Inoue J, Sakaki Y. Serine-proline replacement at residue 127 of NADH-cytochrome b5 reductase causes hereditary methemoglobinemia, generalized type. Blood 1990; 75:1408–13.
- Kugler W, Pekrun A, Laspe P, Erdlenbruch B, Lakomek M. Molecular basis of recessive congenital methemoglobinemia, types I and II: Exon skipping and three novel missense mutations in the NADH-cytochrome b5 reductase (diaphorase 1) gene. Hum Mutat 2001; 17: 348.
- Lamy M, Frezal J, Jammet ML, Josso N. [Recessive congenital methemoglobinemia.]. Nouv Rev Fr Hematol 1963; 3: 105–20.
- Leroux A, Mota Vieira L, Kahn A. Transcriptional and translational mechanisms of cytochrome b5 reductase isoenzyme generation in humans. Biochem J 2001; 355: 529–35.
- Lostanlen D, Vieira de Barros A, Leroux A, Kaplan JC. Soluble NADH-cytochrome b5 reductase from rabbit liver cytosol: partial purification and characterization. Biochim Biophys Acta 1978; 526: 42–51.
- Manabe J, Arya R, Sumimoto H, Yubisui T, Bellingham AJ, Layton DM, et al. Two novel mutations in the reduced nicotinamide adenine dinucleotide (NADH)-cytochrome b5 reductase gene of a patient with generalized type, hereditary methemoglobinemia. Blood 1996; 88: 3 208 – 15.
- Maran J, Guan Y, Ou CN, Prchal JT. Heterogeneity of the molecular biology of methemoglobinemia: a study of eight consecutive patients. Haematologica 2005; 90: 687–9.
- Nussenzveig RH, Lingam HB, Gaikwad A, Zhu Q, Jing N, Prchal JT. A novel mutation of the cytochrome-b5 reductas gene in an Indian patient: the molecular basis of type I methemoglobinemia. Haematologica 2006; 91: 1542–5.
- Orsini A, Vovan L, Brusquet Y, Gabriel B, Sebag F, Galtier M. Congenital methemoglobinemia due to NADH (DPNH) dependent methemoglobin reductase deficiency. Mars Med 1972; 109: 279–81.
- Owen EP, Berens J, Marinaki AM, Ipp H, Harley EH. Recessive congenital methaemoglobinaemia type II a new mutation which causes incorrect splicing in the NADH-cytochrome b5 reductase gene. J Inherit Metab Dis 1997; 20: 610.
- Percy MJ, Crowley LJ, Davis CA, McMullin MF, Savage G, Hughes J, et al. Recessive congenital methaemoglobinaemia: functional characterization of the novel D239G mutation in the NADH-binding lobe of cytochrome b5 reductase. Br J Haematol 2005; 129: 847–53.
- Ronconi G, Ferracin G. [Congenital methemoglobinemia of the recessive type due to diaphorase deficit with oligophrenia.]. Riv Clin Pediatr 1964; 74: 152–9.
- Roussel A, Maestraggi P, Tremoulet M, Marchand. A new case of recessive congenital methemoglobinemia. Arch Fr Pediatr 1963; 20: 745–50.
- Sacerdotti-Favini. Methemoglobinemia costituzionale con cerebropatia e oligofrenia. Acta pediat Lat 1948; 11: 255.
- Scott EM, Griffith IV. The enzyme defect of hereditary methemoglobinemia: diaphorase. Biochim Biophys Acta.1959;34:584–586.
- Shirabe K, Landi MT, Takeshita M, Uziel G, Fedrizzi E, Borgese N. A novel point mutation in a 3’splice site of the NADH-cytochrome b5 reductase gene results in immunologically undetectable enzyme and impaired NADH-dependent ascorbate regeneration in cultured fibro-blasts of a patient with type II hereditary methemoglobinemia. Am J Hum Genet 1995; 57: 302–10.
- Shonola S. Da-Silva, Imran S. Sajan and Joseph P. Underwood, III. Congenital Methemoglobinemia: A Rare Cause of Cyanosis in the NewbornA Case Report./ Pediatrics, 2003;112;e158-e161.
- Shotelersuk V, Tosukhowong P, Chotivitayatarakorn P, Pongpunlert W. A Thai boy with hereditary Enzymopenic methemoglobinemia type II. J Med Assoc Thai 2000; 83: 1380–6.
- Smith, R. P. Chapter 11, Toxic responses of the blood. In Casarett and Doull's Toxicology. The Basic Science of Poisons, 5th ed., C. D. Klaassen, Ed., McGraw-Hill, New York, 1996.
- Strittmatter P, Spatz L, Corcoran D, Rogers MJ , Setlow B, Redline R. Purification and properties of rat liver microsomal stearyl coenzyme A desaturase. Proc Natl Acad Sci USA 1974; 71: 4565–9.
- Takeshita M, Matsuki T, Tanishima K, Yubisui T, Yoneyama Y, Kurata K, et al. Alteration of NADH-diaphorase and cytochrome b5 reductase activities of erythrocytes, platelets, and leukocytes in hereditary methaemoglobinaemia with and without mental retardation. J Med Genet 1982; 19: 204–9.
- Toelle SP, Boltshauser E, Mossner E, Zurbriggen K, Eber S. Sever neurological impairment in hereditary methaemoglobinaemia type 2. Eur J Pediatr 2004; 163: 207–9.
- Trost C. The blue people of Troublesome Creek. Science 82, November, pp. 35-39, 1982.
- Vieira M, Kaplan JC, Kahn A, Leroux A. Four new mutations in the NADH-cytochrome b5 reductase gene from patients with recessive congenital methemoglobinemia type II. Blood 1995; 85: 2254–62.
- Wang Y, Wu YS, Zheng PZ, Yang WX, Fang GA, Tang YC, et al. A novel mutation in the NADH-cytochrome b5 reductase gene of a Chinese patient with recessive congenital methemoglobinemia. Blood 2000; 95: 3250–5.
- Williamson DA, Black JA. Congenital methaemoglobinaemia; a case report. Great Ormond St J 1954; 7: 56–61.
- Wu YS, Wang Y, Huang CH, Lan FH, Zhu ZY. A compound heterozygote in the NADH-cytochrome b5 reductase gene from a Chinese patient with hereditary methemoglobinemia type I. Int J Hematol 2000;72: 34–6.
- Yawata Y, Ding L, Tanishima K, Tomoda A. New variant of cytochrome b5 reductase deficiency (b5RKurashiki) in red cells, platelets, lymphocytes, and cultured fibroblasts with congenital methemoglobinemia, mental and neurological retardation, and skeletal anomalies. Am J Hematol 1992; 40: 299–305.
- Yilmaz D, Cogulu O, Ozkinay F, Kavakli K, Roos D. A novel mutation in the DIA1 gene in a patient with methemoglobinemia type II. Am J Med Genet A 2005; 133: 101–2.
- Yuksel D, Senbil N, Yilmaz D, Yarali N, Gurer YK A rare cause of mental motor retardation: recessive congenital methemoglobinemia type II. /Turk J Pediatr 2009 Mar-Apr; 51(2):187-9.
- Zorc J, Kanic Z. A cyanotic infant: true blue or otherwise? Pediatr Ann.2001;30:597–601.
